Comité Nobel atribuiu o Prémio Nobel de 2019 em medicina a três investigadores: ao norte- americano William G. Kaelin Jr, da Harvard Medical School, Boston, e do Howard Hughes Medical Institute, Chevy Chase, dos EUA; ao inglês Peter J. Ratcliffe da University of Oxford, Oxford, United Kingdom, Francis Crick Institute, London, do Reino Unido; e ao também norte-americano Gregg L. Semenza, da Johns Hopkins University, Baltimore dos EUA.
Os três investigadores são reconhecidos pelas suas descobertas de como as células podem sentir e se adaptar às mudanças na disponibilidade de oxigénio. Os investigadores identificaram máquinas moleculares que regulam a atividade dos genes em resposta a níveis variados de oxigénio.
Os animais precisam de oxigénio para a conversão de alimentos em energia útil. A importância fundamental do oxigénio é conhecida há vários séculos, mas há muito que não se conhecia como as células se adaptam às mudanças nos níveis de oxigénio.
As descobertas dos investigadores revelaram o mecanismo para um dos processos adaptativos mais essenciais da vida. Eles estabeleceram a base para a compreensão de como os níveis de oxigénio afetam o metabolismo celular e a função fisiológica. As descobertas também abriram o caminho para novas e promissoras estratégias para combater a anemia, o cancro e muitas outras doenças.
Oxigénio no centro do palco
O oxigénio constitui cerca de um quinto da atmosfera da Terra. O oxigénio é essencial para a vida animal: é usado pelas mitocôndrias presentes em praticamente todas as células animais para converter os alimentos em energia útil. Otto Warburg, vencedor do Prémio Nobel de 1931 em Medicina, revelou que essa conversão é um processo enzimático.
Durante a evolução, foram desenvolvidos mecanismos para garantir um abastecimento suficiente de oxigénio aos tecidos e às células. O corpo carotídeo, adjacente aos grandes vasos sanguíneos de ambos os lados do pescoço, contém células especializadas que detetam os níveis de oxigénio no sangue. O Prémio Nobel de Medicina de 1938, Corneille Heymans, mostrou como o oxigénio no sangue através do corpo carotídeo controla nossa frequência respiratória, comunicando-se diretamente com o cérebro.
Fator Induzido por hipoxia entra em cena
Além da rápida adaptação controlada pelo corpo carotídeo a baixos níveis de oxigénio (hipoxia), existem outras adaptações fisiológicas fundamentais. Uma resposta fisiológica chave à hipoxia é o aumento dos níveis do hormônio eritropoietina (EPO), que leva ao aumento da produção de glóbulos vermelhos (eritropoiese). A importância do controlo hormonal da eritropoiese já era conhecida no início do século XX, mas como o processo era controlado pelo oxigénio permaneceu um mistério.
Gregg Semenza estudou o gene EPO e como ele é regulado pela variação dos níveis de oxigénio. Usando ratos modificados o investigador mostrou como segmentos específicos de ADN localizados ao lado do gene EPO mediavam a resposta à hipoxia. Peter Ratcliffe também estudou a regulação dependente do gene da EPO, e ambos os grupos de investigação verificaram que o mecanismo sensor de oxigénio estava presente em praticamente todos os tecidos, e não apenas nas células de rim onde a EPO é normalmente produzido. As descobertas mostrando que o mecanismo era geral e funcional em muitos tipos de diferentes células.
Gregg Semenza pretendia identificar os componentes celulares que mediavam essa resposta, e em células hepáticas cultivadas, descobriu um complexo de proteínas que se liga ao segmento de ADN identificado de maneira dependente de oxigénio. E chamou a esse complexo Fator Induzido por hipoxia (HIF, hypoxia-inducible factor). Iniciaram-se grandes esforços para purificar o complexo HIF e, em 1995, Gregg Semenza conseguiu publicar algumas de suas principais descobertas, incluindo a identificação dos genes que codificam o HIF. Verificou que o HIF consiste em duas proteínas diferentes de ligação ao ADN, os chamados fatores de transcrição, agora denominados HIF-1α e ARNT. Agora, os investigadores passaram a dispor de meios para começar a resolver o quebra-cabeça, permitindo entender quais componentes adicionais que estavam envolvidos e como a maquinaria funciona.
Doença de von Hippel-Lindau: um parceiro inesperado
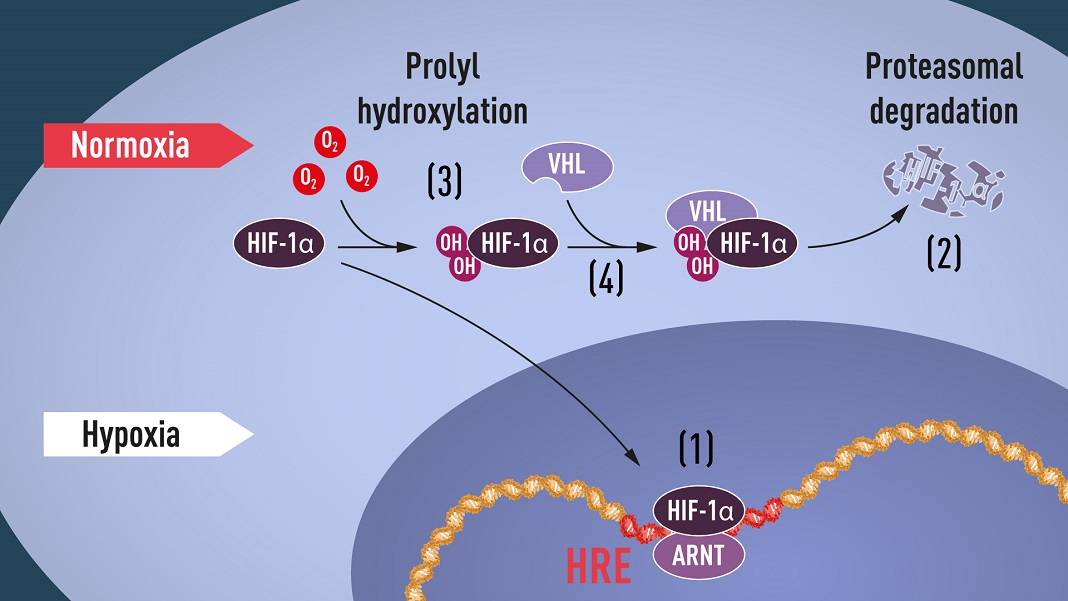
Quando os níveis de oxigénio são altos, as células contêm muito pouco HIF-1a. No entanto, quando os níveis de oxigénio são baixos, a quantidade de HIF-1α aumenta para que possa ligar-se e, assim, regular o gene da EPO, bem como outros genes com segmentos de ADN de ligação ao HIF. Vários grupos de investigação mostraram que o HIF-1α, que normalmente é rapidamente degradado, é protegido da degradação na hipoxia. Em níveis normais de oxigénio, uma máquina celular chamada proteassoma, reconhecida com o Prémio Nobel de Química de 2004 a Aaron Ciechanover, Avram Hershko e Irwin Rose, degrada o HIF-1α. Sob tais condições, um pequeno peptídeo, a ubiquitina, é adicionado à proteína HIF-1α. A ubiquitina funciona como um marcador para proteínas destinadas à degradação no proteassoma. Como a ubiquitina se liga ao HIF-1α de maneira dependente de oxigénio permaneceu uma questão central.
A resposta veio de uma direção inesperada. Na mesma época em que Semenza e Ratcliffe estavam a explorar a regulação do gene EPO, o investigador de cancro, William Kaelin Jr. estava a investigar uma síndrome hereditária, a doença de von Hippel-Lindau (doença de VHL). Esta doença genética leva a um aumento dramático do risco de certos tipos de cancro em famílias com mutações herdadas na VHL. Kaelin mostrou que o gene da VHL codifica uma proteína que impede o aparecimento de cancro. Kaelin também mostrou que as células cancerígenas sem um gene VHL funcional expressam níveis anormalmente altos de genes regulados por hipoxia, mas quando o gene da VHL foi reintroduzido nas células cancerígenas, os níveis normais foram restaurados. Essa foi uma pista importante, mostrando que a VHL estava de alguma forma envolvida no controlo das respostas à hipoxia. Pistas adicionais vieram de vários grupos de investigação, mostrando que a VHL faz parte de um complexo que rotula proteínas com ubiquitina, marcando-as para degradação no proteassoma. Ratcliffe e seu grupo de investigação fizeram uma descoberta importante: demonstrar que a VHL pode interagir fisicamente com o HIF-1α e é necessária para sua degradação em níveis normais de oxigénio. Isso vinculou conclusivamente a VHL ao HIF-1a.
O oxigénio reduz a balança
Muitas peças já estavam no seu no lugar, mas o que ainda faltava era uma compreensão de como os níveis de oxigénio regulam a interação entre BVS e HIF-1α. A investigação concentrou-se numa porção específica da proteína HIF-1α, conhecida por ser importante para a degradação dependente da VHL, e Kaelin e Ratcliffe suspeitaram que a chave para a deteção de oxigénio residisse em algum lugar nesse domínio da proteína. Em 2001, em dois artigos publicados simultaneamente, mostraram que, sob níveis normais de oxigénio, grupos hidroxila são adicionados em duas posições específicas no HIF-1a. Essa modificação proteica, chamada prolil hidroxilação, permite que a VHL reconheça e se ligue ao HIF-1α e, assim, explicou como os níveis normais de oxigénio controlam a degradação rápida do HIF-1α com a ajuda de enzimas sensíveis ao oxigénio (as chamadas prolil hidroxilases). Outras investigações de Ratcliffe e de outros investigadores identificaram as prolil hidroxilases responsáveis. Também foi demonstrado que a função de ativação génica do HIF-1α era regulada por hidroxilação dependente de oxigénio. Os vencedores do Nobel elucidaram o mecanismo e deteção de oxigénio e mostrado como ele funciona.
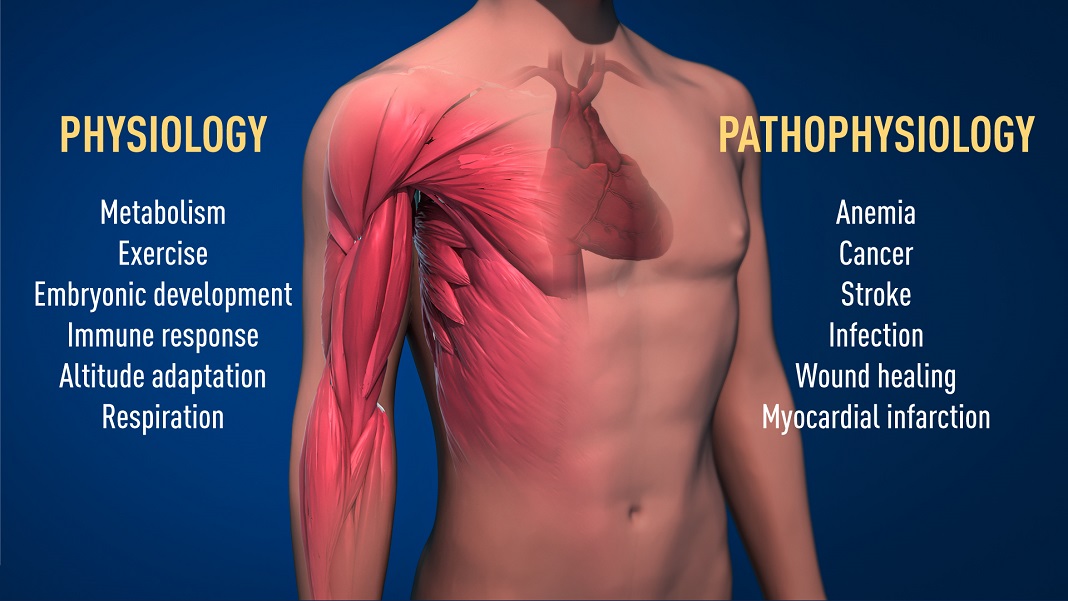
Fisiologia e patologia das formas de oxigénio
Graças ao trabalho inovador desses ganhadores do Nobel, sabemos muito mais sobre como os diferentes níveis de oxigênio regulam os processos fisiológicos fundamentais. A deteção de oxigênio permite que as células adaptem seu metabolismo a baixos níveis de oxigênio: por exemplo, em nossos músculos durante exercícios intensos. Outros exemplos de processos adaptativos controlados pela deteção de oxigênio incluem a geração de novos vasos sanguíneos e a produção de glóbulos vermelhos. Nosso sistema imunológico e muitas outras funções fisiológicas também são aperfeiçoadas pelo mecanismo de deteção de O2. A deteção de oxigênio mostrou-se essencial durante o desenvolvimento fetal para controlar a formação normal dos vasos sanguíneos e o desenvolvimento da placenta.
A deteção de oxigênio é central para um grande número de doenças. Por exemplo, pacientes com insuficiência renal crónica geralmente sofrem de anemia grave devido à diminuição da expressão da EPO. A EPO é produzida por células nos rins e é essencial para controlar a formação de glóbulos vermelhos. Além disso, a maquinaria regulada por oxigénio tem um papel importante no cancro. Nos tumores, a maquinaria regulada por oxigénio é utilizada para estimular a formação de vasos sanguíneos e remodelar o metabolismo para uma proliferação eficaz de células cancerígenas. Os intensos esforços contínuos em laboratórios académicos e empresas farmacêuticas estão agora focados no desenvolvimento de medicamentos que podem interferir com diferentes estados de doenças, ativando ou bloqueando o mecanismo de deteção de oxigénio.